我們看到全球基因研究的資源分配不均。與擁有近千萬筆歐裔數據的資料庫比較,非歐裔基因組研究顯得落後。「缺乏多樣性」的問題不僅加劇族群之間醫療健康差距和不平等,也導致研究失衡,讓科學家錯失重要科學發現。
文/宋明家
好多年前翻閱英文《星報》,讀到一篇讀者治療肺癌的親身經歷。文中提到醫療團隊將他的癌組織樣本送到美國進行「腫瘤基因分析」,以檢測癌細胞DNA、RNA及蛋白質的突變變異,讓主治醫師為他制定個體化治療方案[1]。這個案後來被我納入課堂教材。
癌症目前是我國第三大死因,高發癌症病例包括乳腺癌、結直腸癌、肺癌、淋巴瘤、肝癌等[2]。面對這種發病率持續攀升、日益嚴峻的公共衛生問題,早期篩查、公眾教育、先進治療方案成了必備的戰略武器。關鍵是,癌症治療不存在「放之四海皆准」的標準通用方案,而只有「量體裁衣」的個體化原則。某些疾病可能由單一基因變異導致,如囊性纖維化(cystic fibrosis)。但大多數人類疾病,如癌症、心憂鬱症、心血管疾病等都很複雜,涉及很多基因變異及生活方式、環境因素的綜合作用;單靠幾個基因來判斷醫療方案,其療效很有限。

隨著生物科技的不斷進化和演變,現代醫學界慢慢進化至全基因組解析、結合「多基因風險評分」(polygenic risk scores ,簡稱PRS)技術的醫療方式,以識別疾病中的遺傳因素,來評估某人罹患特定疾病的風險,以及幫助醫療團隊依據「精准醫療」策略,確定在特定病程階段對患者最好的療法。許多基因包括PIK3CA、ERBB2、FGFR、BRAF變異的發現,促進了更精准的「靶向治療藥物」研發,以阻斷癌症進展[3]。
PRS技術有賴於全球科學家這十多年來致力於「全基因組關聯研究」(GWAS)。這套技術通過大量基因組鑒定可能增加或降低疾病風險的變異DNA。這意味著只要把這些微小遺傳差異的影響力疊加、統計,就可計算病人PRS評分,以精准識別疾病風險水平。目前,PRS檢測可靠性越來越強,量身訂造的相應醫療方案,也越來越高效。
當然,PRS不是萬能藥,主治醫師還必須結合其他「非基因」的種族、生理、家族病史、環境因素、生活方式、疾病前驅臨床特徵等種種條件和資訊,來進行較全面的綜合評估。由於GWAS研究依賴大量「基因組」和「表型」(phenotype)數據[4],去識別DNA和疾病之間的關聯,再把非基因因素納入考量,以尋找最合適的醫療方案。醫學界目前面對的問題是,亞洲和其他非歐裔群體「基因組」和「表型」數據的嚴重匱乏。
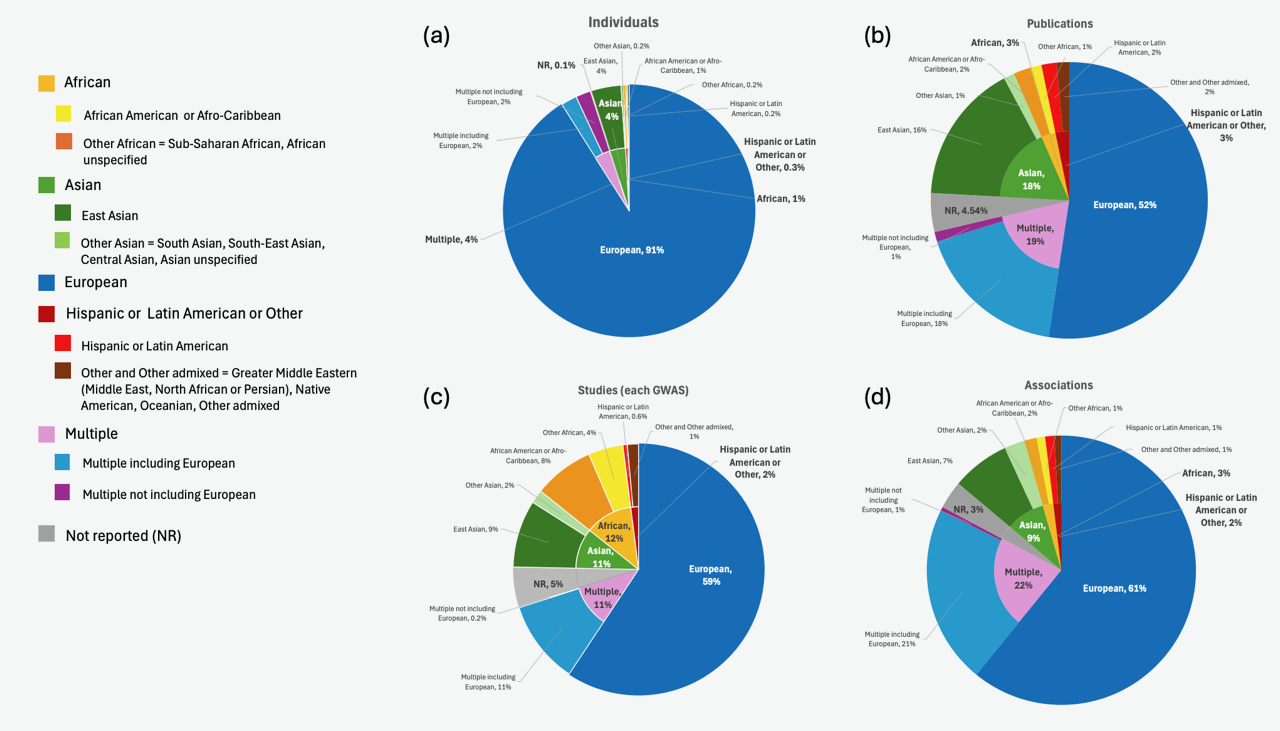
根據英國權威生物信息學研究中心EMBL(歐洲分子生物學實驗室)2024年數據,全世界GWAS研究中的亞洲人群僅佔4%,歐裔則是91%[5]。這幾年非歐裔基因組研究數量確有提升趨勢。比如,韓國Kangwon National University School of Medicine和基因組測序公司Macrogen在2023年8月發佈的1萬1千個亞洲人基因組分析結果[6]。另外,由新加坡國家精准醫療計劃(National Precision Medicine Programme)協調的10萬新加坡人基因組測序SG100K項目,已於今年6月完成10萬個基因組測序[7]。經多年努力,中國近年持續擴大基因組測序規模,目前已建設126 萬人樣本,構建了精准醫學研究的框架和大數據平台[8]。我國去年則剛啓動一項解析各族群遺傳構成的MyGenom計劃[9]。這個基因組測序項目雖略顯緩慢,但希望我國未來幾年內會有至少一萬筆數據,以推動精准醫療研究。
European Molecular Biology Laboratory
縱觀以上數據,我們看到全球資源分配不均。與擁有近千萬筆歐裔數據的資料庫比較,非歐裔基因組研究顯得落後。「缺乏多樣性」的問題不僅加劇族群之間醫療健康差距和不平等,也導致研究失衡,讓科學家錯失重要科學發現。從遺傳學角度來看,非洲和南亞人群擁有全人類最豐富的遺傳多樣性。因此,缺少這些人群的基因組數據,意味著科學家將和豐富的基因資訊失之交臂,無法協助深入理解遺傳疾病[10]。此前,美國University of Maryland School of Medicine利用共11000人的非洲群體基因組數據進行PRS分析。研究人員針對腰臀比(waist-hip ratio)、腰圍、BMI和身高開展GWAS研究,發現多個相關新DNA變異,凸顯多樣化基因組的重要性[11]。
遺憾的是,目前非裔群體基因組研究佔比,只有區區12%,和亞洲人同病相憐。另,根據美國Broad Institute of Harvard and MIT研究發現,基於歐洲人群構建的PRS模型,在南亞、東亞和非洲人群的預測準確度分別降低1.6、2.0和4.5倍[12]。
這些問題,不能僅僅通過增加亞洲或非洲人的基因組數量而獲得解決。人類絕大多數疾病和生理性狀盤根錯節。各個基因和非基因生理與環境因子相互制衡、相互影響。少了表型數據,就算空有數百萬個基因組,GWAS研究還是「英雄無用武之地」,終究無法提高PRS功效。因此,最終仍需「雙劍合璧」的進行類似新加坡精准醫療計劃的妥善策劃。
無論如何,我國MyGenom計劃是一個好的開端。這項計劃避免國內精准醫療科技進展在未來幾年內,不會太過落後於全球發達國家水平。
[1] 詳見《星報》2019年7月25日,題為‘Aim for personalised treatment of cancer’讀者來信:https://www.thestar.com.my/opinion/letters/2019/07/25/aim-for-personalised-treatment-of-cancer
[2] 詳見https://www.thestar.com.my/starpicks/2025/07/31/targeted-approach-to-cancer-care。
[3] 引自2024年12月《Cancer Treatment and Research Communications》期刊文章,https://doi.org/10.1016/j.ctarc.2024.100860
[4] 表型數據是指身高、體重、血壓、臨床疾病等生理資訊。
[5] 詳見https://www.ebi.ac.uk/gwas/docs/ancestry-data 。
[6] 詳見《Science Advances》期刊論文,https://doi.org/10.1126/sciadv.adg6319
[7] 詳見https://medicine.nus.edu.sg/trp/precision-medicine
[8] 詳見《中國精准醫學2035發展戰略》,中國科學出版社 2023出版,https://academics.casad.cas.cn/cbw/zgxkjqyly2035fzzlcs/jzyx/202310/P020240605538570410867.pdf 。
[9] 詳見https://mygenom.gov.my/en/ 。
[10] 比如某些疾病的「基因功能缺失型變異」(loss-of-function variants)。
[11] 引自2024年10月《Obesity》期刊論文,https://doi.org/10.1002/oby.24123 。
[12] 引自2019年3月《Nature Genetics》研究,https://doi.org/10.1038/s41588-019-0379-x 。
 宋明家 |
出身於馬來西亞吉蘭丹州蕉風椰林的古板可憐(Kubang Kerian)。原以為會終一生古板可憐,因貪戀校園混了個碩士,被中學生再教育兩年,爾後重返實驗室和DNA鬼混,博士畢業後吉人天相得以在某國外大學分校任高級講師。愛好枕戈待旦於雜草稻的分子遺傳演化,遵循儒林生存法則小有發表學術論文數十篇。某年突然發現手指也可以拼出方塊字,從此欲罷不能,每逢周末晚文火煎煮一幅幅五千年古老圖像,在華文報章熬制成評論、科普、雜文等百餘篇,聊以顧影自憐也自娛。 |
本文內容係作者個人觀點,不代表當代評論立場。
喜歡這篇文章請按贊和追踪當代評論臉書專頁,給予我們支持與鼓勵!





